IA
A calibração do tempo usando DNA mitocondrial (mtDNA), baseada no conceito de "relógio molecular", enfrenta diversos problemas e limitações que afetam a precisão das estimativas de datação. Os principais desafios incluem:
Taxa de mutação inconsistente: O princípio do relógio molecular assume uma taxa de mutação constante ao longo do tempo e entre diferentes linhagens, mas estudos mostram que essa taxa pode ser bastante errática e variar significativamente entre espécies e até mesmo entre diferentes regiões do genoma mitocondrial.
Variações nas pressões seletivas: A seleção natural pode limitar ou favorecer mutações genéticas específicas em certas linhagens, o que distorce a acumulação constante de mutações esperada pelo modelo do relógio molecular.
Representação de linhagem única: O mtDNA representa apenas uma única linhagem genética (materna), que pode não ser típica da história evolutiva geral do genoma nuclear completo. Isso significa que a história traçada pelo mtDNA pode não refletir com precisão a história de toda a população ou espécie.
Problemas de calibração com fósseis/dados arqueológicos: A precisão da datação molecular depende da calibração com eventos datados de forma independente (como fósseis ou eventos geológicos). Incertezas nessas datas de calibração de referência introduzem erros nas estimativas de tempo molecular.
Heteroplasmia: A presença de diferentes variantes de mtDNA dentro do mesmo indivíduo ou tecido (heteroplasmia) pode complicar a análise e interpretação dos dados evolutivos e de datação.
Reparo de DNA e outros processos celulares: Fatores como a eficiência dos mecanismos de reparo do DNA podem influenciar a taxa de mutação observada, introduzindo mais uma variável na calibração do tempo.
Devido a esses fatores, as estimativas de datas baseadas em mtDNA podem ser altamente propensas a erros e, muitas vezes, precisam ser vistas com cautela e complementadas com outras linhas de evidência (como dados do DNA nuclear e registros fósseis).
https://www.nature.com/articles/s41598-021-84583-1
Taxa de evolução molecular humana, dependência temporal e efeitos de polimorfismo transitório observados através de genomas de DNA mitocondrial antigos e modernos.
Relatórios científicos 11 , Número do artigo: 5036 ( 2021 )
Resumo
A genética evolutiva humana fornece uma estrutura cronológica para interpretar a história da humanidade. Ela se baseia na hipótese do relógio molecular, que pressupõe uma relação direta entre a taxa de mutação e a taxa de substituição, independente de outros fatores, como a dinâmica demográfica. Analisando genomas mitocondriais completos de humanos antigos e modernos, mostramos aqui que, ao longo do tempo, a taxa de substituição pode ser significativamente mais lenta ou mais rápida do que a taxa média de mutação da linhagem germinativa, confirmando um efeito de dependência temporal atribuível principalmente a mudanças no tamanho efetivo da população humana, com um crescimento exponencial em tempos recentes. Também detectamos que polimorfismos transitórios desempenham um papel de desaceleração na taxa evolutiva deduzida de árvores intraespecíficas de haplogrupos. Finalmente, propomos o uso das linhagens mais divergentes dentro dos haplogrupos como uma abordagem prática para corrigir essas discrepâncias do relógio molecular.
Conteúdo semelhante sendo visualizado por outras pessoas

Introdução
A genética evolutiva estuda a história humana dentro de um contexto molecular cronológico. Nesse sentido, sua principal ferramenta é o relógio molecular¹, que estabeleceu que a taxa de divergência entre proteínas ou sequências de DNA, medida como diferenças mutacionais entre linhagens, é proporcional ao tempo decorrido desde sua separação inicial. No entanto, estudos posteriores descobriram que o relógio varia com a posição do nucleotídeo ou do aminoácido dentro de uma linhagem, também entre linhagens e, muito mais, entre táxons. Assim, a cada vez, modelos mais sofisticados precisam ser implementados para levar em conta essa heterogeneidade² . Outro problema detectado com essa escala de tempo molecular é que ela varia, intra e interespecificamente, ao longo da história da linhagem examinada³ . Recentemente , o progresso na análise de DNA antigo forneceu pontos calibrados adicionais em diferentes momentos para melhorar as estimativas da taxa evolutiva⁵ . No entanto , pelo menos em humanos , essas melhorias não alteraram substancialmente as taxas evolutivas obtidas anteriormente com sequências modernas⁴ . Além disso, as diferenças significativas observadas entre as estimativas da taxa de mutação e da taxa evolutiva não desapareceram quando os marcadores uniparentais foram substituídos pelo sequenciamento massivo de genomas completos 11 , 12 , 13 ou quando a taxa de mutação foi substituída pela taxa de recombinação 14 .
Apesar da incerteza quanto à taxa evolutiva comentada acima, a genética desempenha um papel fundamental na interpretação da história humana. Assim, quando a arqueologia situa a origem dos humanos modernos há mais de 300.000 anos (a.a.) 15 , 16 , ou sua expansão eurasiática a partir da África há mais de 120.000 a.a. 17 , 18 , 19 , datas significativamente mais antigas do que as estimativas genéticas (150.000–200.000 e 50.000–60.000, respectivamente), as descobertas arqueológicas são consideradas geneticamente irrelevantes, pois podem não ter contribuído para o conjunto genético das populações humanas atuais.
Contra essa visão, sugerimos que, aceitando uma dependência da taxa de divergência na dinâmica demográfica passada e confiando na taxa média de mutação da linha germinativa como um valor confiável, é possível reconciliar as datas arqueológicas com as genéticas 20 .
Além disso, veremos que a persistência de uma linhagem ancestral em uma população ao longo das gerações, apesar da taxa de mutação do mtDNA ser relativamente rápida, afeta fortemente a precisão das estimativas da idade de coalescência intraespecífica.
Neste estudo, ao comparar sequências de mitogenomas antigos e modernos, confirmamos que as taxas evolutivas variam notavelmente ao longo do tempo, atingindo valores significativamente mais lentos e mais rápidos do que a taxa média de mutação da linhagem germinativa. Assim, existe um efeito de dependência temporal na taxa evolutiva, com aceleração crescente nos tempos recentes. Também detectamos que polimorfismos transitórios desempenham um papel de desaceleração na taxa evolutiva estimada a partir de árvores filogenéticas. Propomos o uso das linhagens mais divergentes dentro dos haplogrupos como uma abordagem prática para corrigir essas incertezas.
Resultados
taxa de evolução molecular
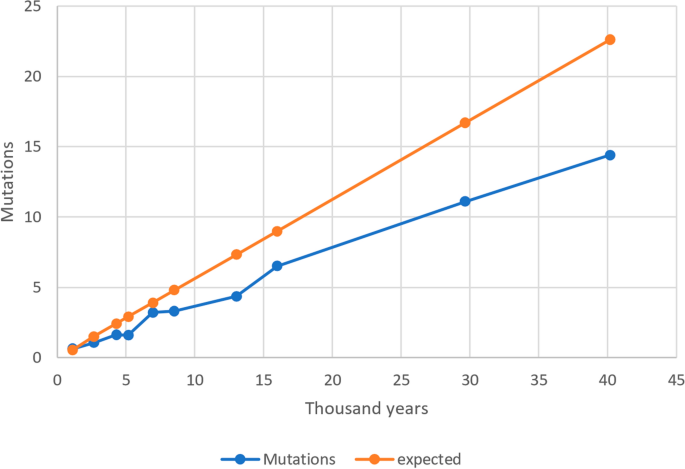
Utilizamos 423 mitogenomas antigos (Tabela Suplementar 1 ) e 784 mitogenomas modernos (Tabelas Suplementares 2 e 3) para estimar a taxa de evolução mitocondrial. Os mitogenomas antigos foram subdivididos em dez períodos de acordo com suas respectivas idades calibradas. As idades médias por período variaram de 1119 ± 483 anos AP a 40.160 ± 4658 anos AP (Tabela 1 ). Não observamos diferenças significativas ao comparar o número médio de diferenças de mutação entre as sequências modernas e antigas para cada macrohaplogrupo (M, N e R) dentro dos períodos. O teste t não pareado para a comparação mais divergente apresentou um valor p de 0,54. Essa homogeneidade entre os haplogrupos reforça a confiabilidade estatística dos valores totais obtidos. As taxas evolutivas observadas variam de 4,33 × 10⁻⁸ ( IC 95% 3,90–4,82 × 10⁻⁸ ) mutações por sítio por ano (ms) para o período mais recente a 1,91 × 10⁻⁸ ( IC 95% 1,72–2,10 × 10⁻⁸ ) ms para o período mais antigo (40.160 ± 4.658 anos atrás). Se igualássemos a primeira estimativa às últimas taxas de mutação da linhagem germinativa publicadas, 1,30 × 10⁻⁸²¹ ou 1,89 × 10⁻⁸ ms²² , nossa taxa seria mais rápida por um fator entre 2,27 e 3,33 vezes, respectivamente . Entretanto, a taxa obtida a partir do período mais antigo de 1,91 × 10 –8 (IC 95%: 1,72–2,10 × 10 –8 ), está na faixa inferior das calculadas por outros autores 7 , 8 , 9 , 10 , 23 , 24 (Tabela 2 ).
Efeito de dependência temporal
Assumindo uma acumulação linear de mutações ao longo do tempo, esperaríamos a mesma taxa de mutação tanto para o período mais recente quanto para o mais antigo, mas, na realidade, o valor observado para o período mais antigo é 2,27 vezes menor do que o calculado para o mais recente. Isso é compatível com a existência de um efeito de dependência temporal nas estimativas de taxa, com taxas de substituição significativamente mais rápidas em tempos recentes em comparação com os mais antigos, como observado por outros autores em humanos e outras espécies 3 , 4 , 7 , 25. Esse efeito é representado graficamente na Figura 1 , onde o número observado e esperado de mutações acumuladas ao longo dos períodos é plotado em função do tempo medido em milhares de anos. De fato, observamos uma regressão significativamente negativa da idade de cada período em relação à taxa evolutiva observada no mesmo período (R = − 684,8; p = 0,0001).
Efeito de polimorfismo transitório
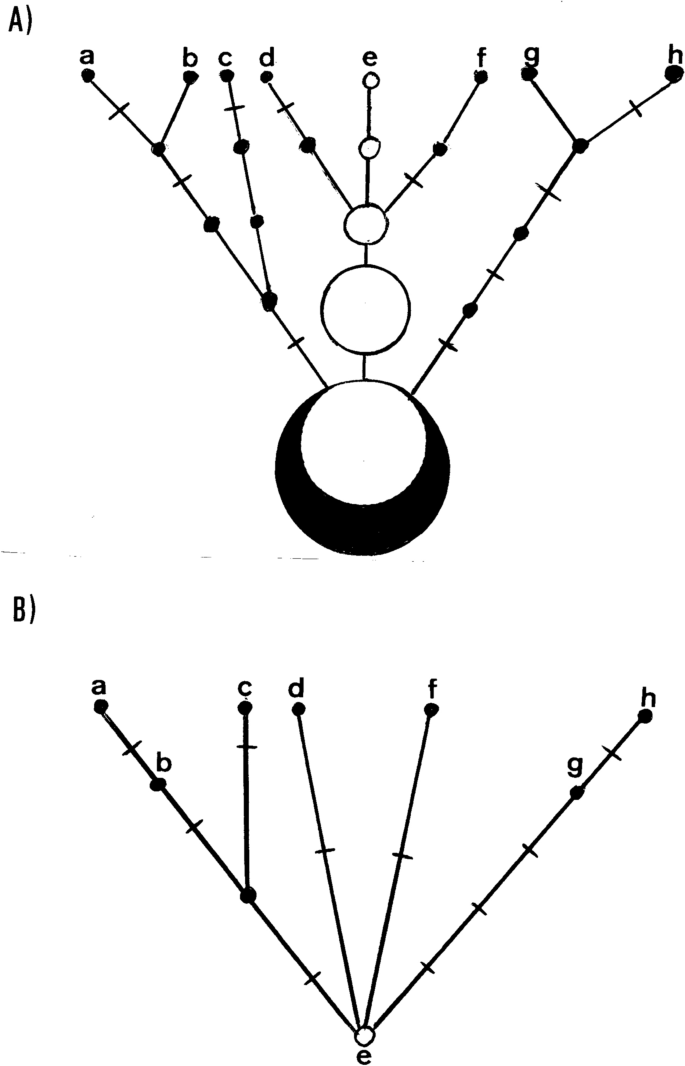
Vimos em “ Métodos ” que a persistência de um polimorfismo transitório do mtDNA se aproxima de 2Ne, portanto, supondo um tamanho efetivo de 5.000 mulheres em humanos, o processo duraria cerca de 10.000 gerações ou, considerando um tempo médio de geração de 25 anos, em torno de 2,5 × 10⁵ anos . Uma consequência imediata é que, em uma população crescente como a humana²⁶ , o tempo de fixação e, portanto, a persistência de um polimorfismo transitório seriam ainda maiores²⁷ . Portanto, espera-se que, apesar da diversidade mitogenômica geralmente alta encontrada em populações humanas, possa haver grandes conjuntos de indivíduos compartilhando o mesmo mitogenoma²⁸ . Por exemplo, um estudo de mtDNA antigo corroborou empiricamente a persistência de uma linhagem M ancestral inalterada ao longo de um período de mais de 8.000 anos²⁹ . Além disso, usando uma calculadora online de distribuição de Poisson ( https://www.stattrek.com ) e uma taxa média de sucesso de mutação de 1,947 × 10⁻⁴ por genoma por ano, a probabilidade de um mitogenoma ancestral não sofrer nenhuma mutação em um período de 12.500 anos (P(x) = 0) ainda não é significativa (P = 0,08771), o que é muito semelhante ao limite de 500 meiose/gerações (12.500 anos assumindo 25 anos por geração) encontrado como o tempo em que dois indivíduos que compartilham o mesmo mitogenoma em uma população são relacionados matrilinealmente²⁸ . Esse período pode aumentar nos casos em que uma população sofre um grande gargalo populacional ou quando uma nova população é fundada a partir de poucos indivíduos e apenas uma única linhagem ou uma linhagem majoritária permanece. Consequentemente, uma linhagem pode permanecer imutável por várias gerações, enquanto linhagens idênticas na mesma população sofrem uma ou várias alterações mutacionais no mesmo intervalo de tempo. Representamos esse cenário na Figura 2A como uma genealogia materna. Observe que a linhagem ancestral pode dar origem a descendentes em diferentes gerações ao longo de sua existência na população. Dessa forma, quando a população é amostrada após n gerações, podemos encontrar, além da linhagem ancestral (e), linhagens derivadas dela que acumularam diferenças mutacionais significativas em seus ramos (f, h). No entanto, esse fato não se reflete na árvore construída a partir da mesma amostra (Figura 2B ), pois, independentemente da geração em que surgiram, todas as linhagens derivadas brotam simultaneamente do nó ancestral (e). Essa diferença entre genealogias e árvores tem consequências notáveis. Por um lado, poderia explicar a falta de homogeneidade na taxa de mutação entre linhagens encontrada em comparações de haplogrupos intraespecíficos 30 , 31 , 32 , 33sem a necessidade de invocar restrições seletivas 34. Por outro lado, a falta de representação das gerações passadas sem impacto mutacional nas linhagens a partir das quais as árvores são construídas tem o efeito geral de encurtar as idades de coalescência calculadas a partir dessas árvores.
Comparação entre uma genealogia ( A ) e uma árvore ( B ) construídas a partir da mesma amostra (a a h). Os círculos brancos representam indivíduos com a linhagem ancestral, os círculos pretos representam indivíduos com mutações adicionais. Os segmentos entre os círculos representam gerações e as cruzes nos segmentos representam mutações.
Uma maneira simples de atenuar esse efeito de encurtamento é escolher as sequências com o maior número de mutações dos haplogrupos analisados em vez da média de suas sequências ou, levando em consideração a variância da distribuição de Poisson, usar a média das sequências agrupadas no primeiro quartil. Na Tabela Suplementar 3, agrupamos as sequências com o maior número de mutações para os principais haplogrupos que constituem os macrohaplogrupos africanos L0 e L3 e os macrohaplogrupos M, N e R, originários de outras regiões da África. Com esses dados e utilizando as taxas evolutivas mencionadas em “ Métodos ”, calculamos as idades de coalescência para episódios importantes da história humana, como a idade dos humanos modernos (divisão L0–L1′2′3′4′5′6′7), a saída da África (divisão L3′4), o retorno das populações eurasiáticas à África (coalescência L3), a expansão dos humanos modernos por toda a Eurásia (coalescências M, N e R), com ênfase especial na colonização do Sahul (coalescência P), da Europa (coalescência U5) e das Américas (coalescências A2, B2, C1, D1, D4h3a e X2a). Como esperado, todas essas novas estimativas são significativamente mais antigas do que as calculadas anteriormente (Tabela 3 ).
Discussão
Embora a taxa de mutação do mtDNA, apesar das variáveis ambientais e genéticas às quais está sujeito 35 , se aproxime de um valor médio consensual 21 , 22 , verificamos aqui que a taxa de substituição do mtDNA varia ao longo do tempo e pode ser menor ou maior que a taxa de mutação. Assim, chegamos à mesma situação que para o genoma completo, para o qual se constatou que a taxa evolutiva dobra a taxa de mutação 11, questionando a cronologia da evolução humana 36 , 37. No entanto, deveríamos esperar que isso ocorresse se admitirmos que a taxa evolutiva depende do tamanho da população 20 e que houve enormes diferenças no tamanho da população humana ao longo de sua história demográfica, com crescimento populacional explosivo nos tempos recentes 26. Essa aparente contradição com a teoria neutra da evolução molecular merece alguns esclarecimentos. O primeiro é diferenciar entre a taxa de transmissão e a taxa de fixação.
Quando uma mutação surge em uma população de tamanho N₀ , ela tem uma probabilidade de ser transmitida para a próxima geração (N₁ ) de 1/N₀ e uma probabilidade de fixação, dado que seja transmitida, de 1/N₁ . Se o tamanho da população permanecer constante ao longo das gerações (N₀ = N₁ ) , a probabilidade de transmissão e a probabilidade de fixação são as mesmas, exatamente como previsto pela teoria neutra³⁸ . No entanto, quando o tamanho da população flutua ao longo das gerações, a probabilidade de transmissão se comporta de maneira oposta à probabilidade de fixação. Suponha que o tamanho da população dobre na próxima geração (N₁ = 2N₀ ) ; então, a probabilidade de transmissão é 2/N₀ ( ela tem duas chances de ser transmitida). Contudo, a probabilidade de fixação da mutação, dado que ela seja transmitida, é 1/ 2N₀ . Pelo contrário, se a população diminuir pela metade na próxima geração (N₁ = N₀ / 2), a probabilidade de transmissão é 1/2N₀, mas a probabilidade de fixação, dado que a mutação seja transmitida, é 2/N₀ . Novamente, isso está de acordo com a teoria neutra, que prevê que, em uma população grande, a probabilidade de fixação de uma mutação é menor do que em uma população pequena. No entanto, é a taxa de transmissão que determina a taxa evolutiva.
Quando estimamos a taxa evolutiva entre populações ou espécies, estamos contabilizando as diferenças de mutação entre as sequências, independentemente de essas variantes serem fixadas para diferentes alelos ou segregarem como polimorfismos transitórios em cada população/espécie. Portanto, o que realmente importa é a quantidade de variação acumulada independentemente em cada linhagem. De fato, as mutações surgem de acordo com a taxa de mutação, mas sabe-se que em uma população em crescimento há mais linhagens, mais mutações se acumulam por linhagem e essas linhagens são mantidas por mais tempo do que em uma população em declínio 27 , 39. Isso explica por que, em uma população em crescimento, a taxa evolutiva acelera e pode ser maior do que a taxa de mutação, uma vez que as mutações que surgem têm maior probabilidade de serem transmitidas e aquelas que já segregam na população permanecem polimórficas por mais tempo. O oposto ocorre em uma população em declínio.
O efeito de dependência temporal, confirmado aqui pela análise comparativa de mitogenomas antigos e modernos, corrobora empiricamente os argumentos expostos acima sobre a dependência da taxa de divergência na dinâmica do tamanho populacional. É indubitável que a seleção também desempenha um papel importante na taxa de evolução, como demonstrado repetidamente pelas diferenças na taxa evolutiva de substituições sinônimas versus não sinônimas 40 , 41 , 42. No entanto, seu efeito pode ser explicado pela teoria quase neutra da evolução molecular, que atribui à deriva genética o papel principal na evolução molecular 43 .
Finalmente, embora tenhamos proposto em outro trabalho um novo algoritmo para contrabalançar os efeitos do crescimento exponencial observado na população humana <sup>20</sup> , ele se baseia na topologia da árvore que agrupa as linhagens amostradas. No entanto, mostramos aqui que as árvores ignoram a persistência das linhagens ancestrais ao longo do tempo, resultando em idades de coalescência mais jovens do que as reais. Embora tenhamos proposto considerar as linhagens com o maior número de mutações dentro de cada haplogrupo em vez da média, como uma abordagem prática para estimar os tempos reais de coalescência, modelos mais sofisticados devem ser implementados para lidar com os problemas que as flutuações no tamanho da população e as restrições da árvore impõem à taxa evolutiva.
Não obstante, vale mencionar que as duas abordagens propostas por nós indicaram tempos de coalescência para a origem dos humanos modernos em torno de 300.000 anos atrás (Tabela 3 ), o que está mais de acordo com descobertas arqueológicas recentes <sup> 15,16 </sup> . Com um atraso semelhante, a saída dos humanos modernos da África foi estimada em cerca de 150.000 anos atrás, um período que poderia coincidir com os registros arqueológicos de Skull e Hafez ou mesmo com os da caverna de Misliya, em Israel <sup> 18,19 </sup> . Além disso, a coalescência dos macro-haplogrupos eurasiáticos M, N e R atrasaria a ocupação humana da Eurásia em cerca de 100.000 anos atrás, o que coincide com a idade estimada para restos dentários humanos escavados na China <sup>44</sup> . A divisão do haplogrupo australasiano P parece indicar que os humanos modernos chegaram a Sahul ao mesmo tempo que ao leste da Ásia (Tabela 3 ). Como parte dessa expansão contemporânea, as populações eurasiáticas também podem ter retornado à África coincidindo com a divisão africana L3 (Tabela 3 ) 45. Finalmente, embora tenhamos proposto uma migração única para a colonização das Américas há cerca de 40.000 anos 20 , que é direta ou indiretamente apoiada por datas arqueológicas 46 , 47 , parece possível que essa primeira migração, sinalizada pelas idades dos haplogrupos A2 e B2, tenha sido seguida posteriormente por uma segunda onda, também antes do Último Máximo Glacial, marcada pelos haplogrupos C1, D1, D4h3a e X2a há cerca de 27.500 anos (Tabela 3 ).
A taxa de evolução nos seres humanos permanece uma questão em aberto. No entanto, acreditamos que existem evidências suficientes para questionar as idades propostas pelos geneticistas para os principais eventos da evolução humana.
Métodos
Materiais
Sequências completas de mtDNA humano antigo e moderno disponíveis publicamente foram baixadas dos seguintes bancos de dados: NCBI GenBank ( www.ncbi.nlm.nih.gov/genbank/ ), Mitomap ( www.mitomap.org/MITOMAP ), IanLogan 2020 ( www.ianlogan.co.uk/sequences_by_group/haplogroup_select.htm ) e AmtDB ( http://amtdb.org ) 48 .
Métodos
Os haplótipos de mtDNA extraídos da literatura foram transformados em sequências usando o programa Haplosearch ( http://www.haplosite.com/haplosearch/process/ ) <sup>49</sup> . As sequências foram alinhadas manualmente e comparadas à Sequência de Referência de Cambridge revisada (rCRS) <sup>50 </sup> usando o programa de alinhamento de sequências BioEdit<sup> 51</sup> . A atribuição das sequências aos haplogrupos foi confirmada usando a versão build17 do PhyloTree ( http://www.phylotree.org ) <sup>52</sup> . Inserções e deleções (indels) em torno dos nucleotídeos 309, 522 e 16.193 e a mutação no ponto quente 16.519 foram excluídas de todas as análises. As sequências com o maior número de mutações para cada haplogrupo foram escolhidas, após a análise de alinhamento, dentro de sua faixa máxima, excluindo-se aquelas claramente discrepantes. As sequências antigas puderam ser agrupadas em dez períodos diferentes com tamanho amostral estatístico suficiente. A idade média de cada período antigo foi definida como a média ponderada das idades calibradas de suas sequências. Para cada agrupamento de sequências antigas por período, construímos um grupo moderno equivalente com sequências filogeneticamente equivalentes às presentes no grupo antigo. A idade atribuída a todas as sequências modernas foi de 2000 anos d.C. Para comparar nossas idades de coalescência com as de outros autores, utilizamos a estatística rho 53 e duas taxas de substituição: a proposta por Soares et al. 23, baseada em mitogenomas modernos, corrige a seleção purificadora e assume uma taxa de uma mutação a cada 3624 anos; a outra é uma taxa média calculada por diversos autores utilizando mitogenomas antigos 7 , 8 , 9 , 10 , 24 , resultando em uma mutação a cada 2454 anos.
taxa de evolução molecular
As taxas de evolução molecular (θ) foram calculadas usando o estimador frequentista:
onde d<sub> ij</sub> é o número de diferenças entre pares de sequências modernas e antigas, n é o número total de pares comparados e T é o tempo do período analisado em anos. Partimos do princípio de que, como as mutações ocorrem em sequências seguindo uma distribuição de Poisson, dentro da mesma linhagem, as sequências modernas deveriam acumular mais mutações do que as antigas, conforme previsto pelo relógio molecular<sup> 1 </sup>. Mesmo em nível intraespecífico, a maioria das sequências sofre mutações recorrentes e paralelas, principalmente em posições altamente variáveis, o que poderia levar a uma interpretação errônea do número real de diferenças de mutação entre as sequências. Felizmente, na maioria dos casos, as mudanças de estado dessas posições podem ser mapeadas hierarquicamente, desde os ramos basais até as pontas da árvore filogenética do DNA mitocondrial humano, que apresenta alto contraste<sup> 52 </sup>. As taxas evolutivas para cada período foram calculadas para cada macrohaplogrupo (M, N e R) e para o total, estimadas como a média ponderada das taxas obtidas para cada macrohaplogrupo.
Efeito de dependência temporal
O efeito da dependência temporal na taxa evolutiva foi estimado por meio de regressão entre a idade média de cada período e sua respectiva taxa evolutiva.
Persistência de um polimorfismo transitório
Sob as condições da teoria neutra, o número médio de gerações entre a ocorrência e a fixação de uma mutação, desde que esta não seja fixada durante o processo, foi calculado como 4Ne 54. O valor é reduzido para 2Ne em um sistema haploide como o mtDNA. Este é também o tempo médio de persistência de um polimorfismo transitório. Por outro lado, novas mutações surgirão em sequências individuais a uma taxa de mutação µ durante um intervalo temporal dT, seguindo uma distribuição de Poisson.
As estimativas mais recentes da taxa de mutação do mtDNA da linhagem germinativa humana são de 1,30 × 10⁻⁸ 21 ou 1,89 × 10⁻⁸ 22 mutações por sítio por ano (assumindo um tempo de geração de 25 anos). Consequentemente, estamos usando aqui uma taxa média de sucesso de mutação de 1,947 × 10⁻⁴ por genoma por ano.
Referências
Zuckerkandl, E. & Pauling, L. Genes e proteínas em evolução 97–166 (Elsevier, Amsterdã, 1965).
Arenas, M. Tendências em modelos de substituição da evolução molecular. Front. Genet. 6 , 319 (2015).
Ho, SYW, Phillips, MJ, Cooper, A. & Drummond, AJ Dependência temporal das estimativas de taxas moleculares e superestimação sistemática dos tempos de divergência recentes. Choos. Appropri. Subst. Models Phylogenet. Anal. Protein-Coding Seq. 22 , 1561–1568 (2005).
Henn, BM, Gignoux, CR, Feldman, MW & Mountain, JL Caracterizando a dependência temporal das estimativas da taxa de mutação do DNA mitocondrial humano. Mol. Biol. Evol. 26 , 217–230 (2009).
Leonardi, M. et al. Padrões e processos evolutivos: Lições do DNA antigo. Syst. Biol. 66 , e1–e29 (2017).
Tong, KJ, Duchêne, DA, Duchêne, S., Geoghegan, JL & Ho, SY Uma comparação de métodos para estimar taxas de substituição a partir de dados de sequência de DNA antigo. BMC Evol. Biol. 18 , 1–10 (2018).
Rieux, A. et al. Calibração aprimorada do relógio mitocondrial humano usando genomas antigos. Mol. Biol. Evol. 31 , 2780–2792 (2014).
Fu, Q. et al. Uma escala de tempo revisada para a evolução humana baseada em genomas mitocondriais antigos. Curr. Biol. 23 , 553–559 (2013).
Posth, C. et al. Genomas mitocondriais do Pleistoceno sugerem uma única grande dispersão de não africanos e uma renovação populacional no final do período glacial na Europa. Curr. Biol. 26 , 827–833 (2016).
Brotherton, P. et al. Genomas do haplogrupo H mitocondrial neolítico e as origens genéticas dos europeus. Nat. Commun. 4 , 1764 (2013).
Scally, A. & Durbin, R. Revisando a taxa de mutação humana: implicações para a compreensão da evolução humana. Nat. Rev. Genet. 13 , 745–753 (2012).
Conrad, DF et al. Variação nas taxas de mutação em todo o genoma dentro e entre famílias humanas. Nat. Genet. 43 , 712 (2011).
Roach, JC et al. Análise da herança genética em um quarteto familiar por sequenciamento de genoma completo. Science 328 , 636–639 (2010).
Moorjani, P. et al. Um método genético para datação de genomas antigos fornece uma estimativa direta do intervalo de geração humana nos últimos 45.000 anos. Proc. Natl. Acad. Sci. 113 , 5652–5657 (2016).
Richter, D. et al. A idade dos fósseis de hominídeos de Jebel Irhoud, Marrocos, e as origens da Idade da Pedra Média. Nature 546 , 293–296 (2017).
Hublin, J.-J. e outros. Novos fósseis de Jebel Irhoud, Marrocos e a origem pan-africana do Homo sapiens. Natureza 546 , 289–292 (2017).
Harvati, K. et al. Fósseis da caverna Apidima fornecem as primeiras evidências de Homo sapiens na Eurásia. Nature 571 , 500–504 (2019).
Grün, R. & Stringer, CB Datação por ressonância de spin eletrônico e a evolução dos humanos modernos. Arqueometria 33 , 153–199 (1991).
Hershkovitz, I. et al. Os primeiros humanos modernos fora da África. Science 359 , 456–459 (2018).
Cabrera, VM Contrabalançando o efeito dependente do tempo no relógio molecular do DNA mitocondrial humano. BMC Evol. Biol. 20 , 1–9 (2020).
Rebolledo-Jaramillo, B. et al. Efeito da idade materna e gargalo severo da linha germinativa na herança do DNA mitocondrial humano. Proc. Natl. Acad. Sci. 111 , 15474–15479 (2014).
Zaidi, AA et al. Gargalo e seleção na linhagem germinativa e idade materna influenciam a transmissão do DNA mitocondrial em pedigrees humanos. Proc. Natl. Acad. Sci. USA 116 , 25172–25178 (2019).
Soares, P. et al. Correção para seleção purificadora: um relógio molecular mitocondrial humano aprimorado. Am. J. Hum. Genet. 84 , 740–759 (2009).
Fu, Q. et al. Sequência do genoma de um humano moderno de 45.000 anos da Sibéria Ocidental. Nature 514 , 445–449 (2014).
Pereira, SL & Baker, AJ Uma escala de tempo mitogenômica para aves detecta taxas filogenéticas variáveis de evolução molecular e refuta o relógio molecular padrão. Mol. Biol. Evol. 23 , 1731–1740 (2006).
Coventry, A. et al. O resequenciamento profundo revela excesso de variantes raras recentes consistentes com o crescimento populacional explosivo. Nat. Commun. 1 , 1–6 (2010).
Waxman, D. O crescimento populacional aumenta o tempo médio de fixação de mutações neutras e a persistência da variação neutra. Genetics 191 , 561–577 (2012).
Andersen, MM & Balding, DJ Quantos indivíduos compartilham um genoma mitocondrial?. PLoS Genet. 14 , e1007774 (2018).
Hublin, J.-J. e outros. Homo sapiens inicial do paleolítico superior da Caverna Bacho Kiro, Bulgária. Natureza 2 , 1–4 (2020).
Torroni, A. et al. Os quatro clados do haplogrupo L2 do mtDNA evoluem em taxas diferentes? Am. J. Hum. Genet. 69 , 1348–1356 (2001).
Howell, N., Elson, JL, Turnbull, DM & Herrnstadt, C. Sequências de mtDNA do haplogrupo L africano mostram violações da evolução tipo relógio. Mol. Biol. Evol. 21 , 1843–1854 (2004).
Merriwether, DA et al. Haplogrupos M mitocondriais antigos identificados no Pacífico Sudoeste. Proc. Natl. Acad. Sci. 102 , 13034–13039 (2005).
Pierron, D. et al. Mudança na taxa de mutação dentro de haplogrupos mitocondriais eurasiáticos: impacto da seleção e consequências para a datação do assentamento na Europa. PLoS ONE 6 , 2 (2011).
Maca-Meyer, N. et al. Trânsito de DNA mitocondrial entre a Ásia Ocidental e o Norte da África inferido da filogeografia U6. BMC Genet. 4 , 15 (2003).
Ségurel, L., Wyman, MJ e Przeworski, M. Determinantes da variação da taxa de mutação na linha germinativa humana. Anu. Rev. Zumbir. Geneta. 15 , 47–70 (2014).
Callaway, E. Estudos retardam o relógio do DNA humano: estimativas revisadas das taxas de mutação alinham os relatos genéticos da pré-história humana com os dados arqueológicos. Nature 486 , 343–345 (2012).
Gibbons, A. Retrocedendo no tempo: Diminuindo o ritmo da pré-história. (2012).
Kimura, M. A teoria neutra da evolução molecular: uma revisão de evidências recentes. Jpn. J. Genet. 66 , 367–386 (1991).
Gazave, E., Chang, D., Clark, AG & Keinan, A. O crescimento populacional infla o número de mutações deletérias por indivíduo e reduz seu efeito médio. Genetics 195 , 969–978 (2013).
Schmidt, S. et al. Sítios não sinônimos hipermutáveis estão sob seleção negativa mais forte. PLoS Genet. 4 , e1000281 (2008).
Hughes, AL, Friedman, R., Rivailler, P. & French, JO Polimorfismos sinônimos e não sinônimos versus divergências em genomas bacterianos. Mol. Biol. Evol. 25 , 2199–2209 (2008).
Yang, Z. & Nielsen, R. Estimativa de taxas de substituição sinônimas e não sinônimas sob modelos evolutivos realistas. Mol. Biol. Evol. 17 , 32–43 (2000).
Ohta, T. & Gillespie, JH Desenvolvimento de teorias neutras e quase neutras. Theor. Popul. Biol. 49 , 128–142 (1996).
Liu, W. et al. Os primeiros humanos inequivocamente modernos no sul da China. Nature 526 , 696–699 (2015).
Cabrera, VM, Marrero, P., Abu-Amero, KK & Larruga, JM. Portadores de linhagens basais do macrohaplogrupo L3 do DNA mitocondrial migraram de volta para a África da Ásia há cerca de 70.000 anos. BMC Evol. Biol. 18 , 98 (2018).
Pitulko, VV et al. Presença humana precoce no Ártico: Evidências de restos de mamutes de 45.000 anos. Science 351 , 260–263 (2016).
Gruhn, R. Crescem as evidências de que o povoamento das Américas começou há mais de 20.000 anos. (2020).
Ehler, E. et al. AmtDB: Um banco de dados de genomas mitocondriais humanos antigos. Nucleic Acids Res. 47 , D29–D32 (2019).
Fregel, R. & Delgado, S. HaploSearch: Uma ferramenta para transformação bidirecional de sequência de haplótipo. Mitochondrion 11 , 366–367 (2011).
Andrews, RM et al. Reanálise e revisão da sequência de referência de Cambridge para o DNA mitocondrial humano. Nat. Genet. 23 , 147–147 (1999).
Hall, TA et al. BioEdit: um editor de alinhamento de sequência biológica amigável e programa de análise para Windows 95/98/NT. Nucleic Acids Symp. Ser, 41 , 95–98 (1999).
Van Oven, M. & Kayser, M. Árvore filogenética abrangente atualizada da variação global do DNA mitocondrial humano. Hum. Mutat. 30 , E386–E394 (2009).
Forster, P., Harding, R., Torroni, A. & Bandelt, H.-J. Origem e evolução da variação do mtDNA dos nativos americanos: uma reavaliação. Am. J. Hum. Genet. 59 , 935 (1996).
Kimura, M. & Ohta, T. O número médio de gerações até a fixação de um gene mutante em uma população finita. Genetics 61 , 763–771 (1969).
Informações sobre o autor
Autores e Afiliações
Contribuições
VMC, como único autor, concebeu, executou e redigiu o manuscrito.
Autor correspondente
Declarações éticas
Interesses conflitantes
O autor declara não haver conflito de interesses.
Informações adicionais
Nota do editor
A Springer Nature mantém-se neutra em relação a reivindicações jurisdicionais em mapas publicados e afiliações institucionais.
Informações complementares
Direitos e permissões
Acesso Aberto. Este artigo está licenciado sob a Licença Internacional Creative Commons Atribuição 4.0, que permite o uso, compartilhamento, adaptação, distribuição e reprodução em qualquer meio ou formato, desde que você dê o devido crédito ao(s) autor(es) original(is) e à fonte, forneça um link para a licença Creative Commons e indique se foram feitas alterações. As imagens ou outros materiais de terceiros neste artigo estão incluídos na licença Creative Commons do artigo, a menos que indicado de outra forma em uma linha de crédito para o material. Se o material não estiver incluído na licença Creative Commons do artigo e o seu uso pretendido não for permitido por lei ou exceder o uso permitido, você precisará obter permissão diretamente do detentor dos direitos autorais. Para visualizar uma cópia desta licença, visite http://creativecommons.org/licenses/by/4.0/ .
Sobre este artigo
Cite este artigo
Cabrera, VM. Taxa de evolução molecular humana, dependência temporal e efeitos de polimorfismo transitório vistos através de genomas de DNA mitocondrial antigos e modernos. Sci Rep 11 , 5036 (2021). https://doi.org/10.1038/s41598-021-84583-1
Recebido
Aceito
Publicado
Versão do registro
DOIhttps://doi.org/10.1038/s41598-021-84583-1
Comentários
Postar um comentário